איזוטופ
אִיזוֹטוֹפּים של יסוד כימי הם אטומים בעלי אותו מספר אטומי אך בעלי מסה שונה, כלומר מספר הנייטרונים שונה. לאיזוטופים של אותו יסוד יש אותן התכונות הכימיות.
כיום מוכרים למדע מעל 1,000 איזוטופים שונים המשויכים ל-118 היסודות בטבלה המחזורית.
מקורה של המלה איזוטופ, ביוונית: Ισος (איסוֹס) = שווה, Τοπος (טוֹפּוֹס) = מקום, ופירושה "אותו מקום", מקור השם נעוץ בעובדה שאיזוטופים נמצאים באותו מקום בטבלה המחזורית של היסודות.
רקע
[עריכת קוד מקור | עריכה]כל היסודות בנויים מאטומים. האטום בנוי, באופן כללי, מגרעין, המורכב מפרוטונים ונייטרונים הבונים את הגרעין, ומאלקטרונים הסובבים סביב הגרעין. התכונה האטומית המבדילה בין חומר אחד למשנהו, היא מספר הפרוטונים שבגרעין. מספר זה - הקרוי מספר אטומי של היסוד, והמייצג גם את מספר הפרוטונים של יסוד זה - קובע את תכונותיו הכימיות של החומר, וממנו נובעים צבעו, מרקמו, ותכונותיו המכניות.
מספר הנייטרונים שבגרעין, לעומת זאת, יכול להשתנות מבלי לשנות את תכונותיו הכימיות של החומר. פעמים רבות מספרם של הנייטרונים שווה למספר הפרוטונים (בפרט ביסודות הקלים), אך הדבר אינו מחויב. מספר הפרוטונים והנייטרונים גם יחד קובע את המשקל האטומי - הנקרא גם מסה אטומית - של האטום. מסת האלקטרונים קטנה פי כ-2,000 ממסת הפרוטון או הנייטרון ולכן זניחה וניתן להתעלם ממנה.
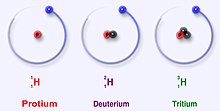
גרעינים שונים של אותו יסוד (כלומר מספר זהה של פרוטונים, אך מספר נייטרונים שונה) נקראים איזוטופים של היסוד. לדוגמה, מימן הוא היסוד הכימי שבגרעין האטום שלו קיים פרוטון אחד בלבד. לרוב, בגרעין מימן אין נייטרונים, ולכן זהו האיזוטופ הנפוץ של מימן. עם זאת, קיימים עוד איזוטופים: גרעין שמכיל פרוטון אחד ונייטרון אחד גם הוא גרעין מימן (בגלל קיום פרוטון בודד) אך זהו איזוטופ שונה שלרוב נקרא דאוטריום או "מימן כבד". בנוסף, קיים איזוטופ נוסף של מימן המכיל שני נייטרונים בגרעין הנקרא טריטיום.
לפעמים איזוטופ מסוים של היסוד מהווה את רוב האטומים של יסוד זה. זהו לדוגמה המצב במימן בו רוב האטומים שלו הם מהאיזוטופ בלי נייטרונים. לעומת זאת, קיימים יסודות בעלי שכיחות דומה של האיזוטופים השונים. לדוגמה, הגז האציל קסנון הוא בעל גרעין עם 54 פרוטונים, וניתן למצוא אותו בטבע בשלושה איזוטופים בעלי תפוצה דומה: 75, 77 או 78 נייטרונים.
בניגוד למימן, שבה לכל איזוטופ יש שם, מרבית האיזוטופים אינם קרויים בשם, אלא קרויים בשם הבנוי משם היסוד ומספר הנוקליאונים (הפרוטונים והנייטרונים שבגרעין) הכולל שבגרעינו. אורניום-238, למשל הוא איזוטופ של אורניום שבגרעינו סך הפרוטונים והנייטרונים ביחד הוא 238. בכתיב הכימי מסומן האיזוטופ בסמל היסוד, שלפניו רשום, בספרות עיליות, מספר הפרוטונים והנייטרונים. 238U, למשל, הוא אורניום-238. עוד דוגמה היא היסוד הכימי פחמן (סימון כימי: C), בעל 6 פרוטונים. 99% מגרעיני הפחמן הם בעלי 6 נייטרונים ולכן מסמנים את האיזוטופ הנפוץ ביותר של פחמן כפחמן-12 או 12C. עם זאת, אחוז מכלל אטומי הפחמן הוא 13C ובאטמוספירה נוצרת כל הזמן כמות מזערית ביותר של 14C שדועכת עם הזמן.
קיומם של איזוטופים שונים לאותו יסוד גורם לכך שהמשקל האטומי, כפי שהוא מופיע בטבלה המחזורית של היסודות, אינו מייצג משקל אטומי של איזוטופ מסוים, אלא את המשקל האטומי המשוקלל, בהתאם לתפוצתם של האיזוטופים בטבע.
אף שלמספר הנייטרונים בגרעין אין השפעה על התכונות הכימיות של היסוד, יש לו השפעה רבה על היציבות של הגרעין - חלק מהאיזוטופים הם איזוטופים רדיואקטיביים. לניקל, למשל, יש 5 איזוטופים יציבים (הגרעין שלהם אינו מתפרק מעצמו), איזוטופ אחד (59Ni) שזמן מחצית החיים שלו הוא יותר מ-10,000 שנה, איזוטופ אחד (63Ni) שזמן מחצית חייו נמדד בשנים רבות ו-3 איזוטופים (56Ni, 57Ni ו-66Ni) שזמן מחצית חייהם הוא פחות מעשרה ימים.
משום שאין הבדלים כימיים בין האיזוטופים השונים של אותו יסוד, לא ניתן להבדיל ביניהם באמצעים כימיים. לדוגמה, כאשר יוצרים מולקולות פחמן דו-חמצני (CO2), כ-99% מהמולקולות יכללו אטום פחמן-12 וכ-1% יכללו פחמן-13, בהתאם לשכיחות שלהם בטבע. כלומר, לאטומי החמצן "לא אכפת" איזה סוג פחמן נקשר אליהם.
שימושי האיזוטופים
[עריכת קוד מקור | עריכה]בין אטומים זהים של אותו יסוד אי אפשר להבדיל בתהליכים כימיים, אך ניתן להבדיל בין איזוטופים שונים בתהליכים פיזיקליים (בעיקר על פי משקלם). יצירת תרכובת מאיזוטופ מסוים מאפשרת מעקב אחר ההתנהגות של האטומים המרכיבים תרכובת זו בתערובת שבה נמצאים אטומים אלה גם בתרכובות אחרות. דוגמה: בחקר התנהגותו של הפנול (C6H5OH) במים, משתמשים במים כבדים (D2O), כלומר מים שהמימן בהם הוא האיזוטופ דאוטריום. בצורה זו ניתן להבחין בין המימן שבפנול ובין המימן שבמים, ולגלות שהפנול המומס במים מחליף אטומי מימן עם המים.
הבדל נוסף אפשרי הוא בתהודה מגנטית גרעינית, אם לאיזוטופ מסוים (כמו 31P, 1H וכו') יש ספין 1/2+ ניתן לראותו במכשיר NMR, או לפחות את האחוז היחסי שלו מתוך היסוד.
לייצורה של פצצת אטום דרושים איזוטופים מסוימים. הפעולה הקרויה "העשרת אורניום" היא בידודו של האיזוטופ הנדיר, 235U, הנחוץ לייצור הפצצה, מתוך האורניום המצוי בטבע שבו האיזוטופ הנפוץ הוא 238U. זהו אתגר טכנולוגי לא פשוט, עקב ההבדלים הפעוטים שבין האיזוטופים.
האיזוטופים 235U ו-239Pu נוחים לביקוע גרעיני, ולפיכך הם משמשים כדלק לכורים גרעיניים וכחומר בקיע בפצצות גרעיניות.
לאיזוטופים הרדיואקטיביים של יסודות רבים (הנקראים רדיו-איזוטופים) יש שימושים במדע בכלל ובביולוגיה בפרט (לרבות המחקר הרפואי) כסַמָּנִים – הודות לכך שאין כל הבדל ממשי בין הפעילות הכימית של האיזוטופים השונים של אותו החומר, ניתן להתחקות אחר התהליכים העוברים על חומר כלשהו בגוף האדם, באמצעות שימוש באיזוטופ הרדיואקטיבי שלו ומדידת הקרינה הנפלטת. לדוגמה, היסוד יוד ממלא תפקיד חשוב בגוף, ובייחוד בפעולתה של בלוטת התריס. בעזרת האיזוטופים הרדיואקטיביים שלו, למשל 135I, אפשר להתחקות אחר מהלך היוד בגוף ולעמוד על סיבותיהן של הפרעות לפעולתה של בלוטה זו.
שימוש אחר לאיזוטופים רדיואקטיביים הוא הפקת חשמל לפי העיקרון התרמו-חשמלי: האנרגיה הנפלטת בהתפרקות מומרת במישרין לזרם חשמלי. התקנים מסוג זה משמשים במקומות שיש בהם צורך בזרם, אך קשה או בלתי-אפשרי לתחזק את מקור הזרם באופן שוטף; לדוגמה, בגשושות חלל או בקוצבי לב.
זמן מחצית החיים של יסודות 83 עד 118
[עריכת קוד מקור | עריכה]כל היסודות בעלי מספר אטומי מעל 82 (עופרת) אינם יציבים, וככלל, זמן מחצית החיים פוחת עם עליית המספר האטומי, החל מהיסוד היציב למדי אורניום (מספר 92) ועד היסוד הכבד ביותר 118. זמן מחצית החיים גדל בתחום היסודות 103 עד 105, יורד ביסוד 106 ועולה שוב קלות ביסודות 110 עד 114, מה שמרמז על היתכנות אי של יציבות.
בטבלה מוצג זמן מחצית החיים של האיזוטופ היציב ביותר של היסוד בטווח.
| מספר אטומי | שם היסוד | האיזוטופ היציב ביתר | מחצית חיים |
|---|---|---|---|
| 83 | ביסמוט | 209Bi | 2 × 1019 שנים |
| 84 | פולוניום | 209Po | 130 שנים |
| 85 | אסטטין | 210At | 8 שעות |
| 86 | רדון | 222Rn | 3.824 ימים |
| 87 | פרנציום | 223Fr | 22.0 דקות |
| 88 | רדיום | 226Ra | 1600 שנים |
| 89 | אקטיניום | 227Ac | 21.77 שנים |
| 90 | תוריום | 232Th | 1.41 × 1010 שנים |
| 91 | פרוטקטיניום | 231Pa | 32800 שנים |
| 92 | אורניום | 238U | 4.47 × 109 שנים |
| 93 | נפטוניום | 237Np | 2.14 × 106 שנים |
| 94 | פלוטוניום | 244Pu | 8.0 × 107 שנים |
| 95 | אמריציום | 243Am | 7400 שנים |
| 96 | קוריום | 247Cm | 1.6 × 107 שנים |
| 97 | ברקליום | 247Bk | 1000 שנים |
| 98 | קליפורניום | 251Cf | 900 שנים |
| 99 | איינשטייניום | 252Es | 470 ימים |
| 100 | פרמיום | 257Fm | 100.5 ימים |
| 101 | מנדלביום | 258Md | 51.5 ימים |
| 102 | נובליום | 259No | 58 דקות |
| 103 | לורנציום | 266Lr | ~11 שעות |
| 104 | רתרפורדיום | 267Rf | ~1.3 שעות |
| 105 | דובניום | 268Db | 1.3 ימים |
| 106 | סיבורגיום | 269Sg | ~3.1 דקות |
| 107 | בוהריום | 270Bh | 3.8 דקות |
| 108 | האסיום | 277mHs | ~130 שניות |
| 109 | מייטנריום | 278Mt | 7.6 שניות |
| 110 | דרמשטטיום | 281mDs | ~3.7 דקות |
| 111 | רנטגניום | 282Rg | 2.1 דקות |
| 112 | קופרניקיום | 285mCn | ~8.9 דקות |
| 113 | ניהוניום | 286Nh | 19.6 שניות |
| 114 | פלרוביום | 289mFl | ~1.1 דקות |
| 115 | מוסקוביום | 289Mc | 220 מילי-שניות |
| 116 | ליברמוריום | 293Lv | 61 מילי-שניות |
| 117 | טנסין | 294Ts | 78 מילי-שניות |
| 118 | אוגאנסון | 294Og | 890 מיקרו-שניות |
