Malattia di Charcot-Marie-Tooth
La malattia di Charcot-Marie-Tooth o CMT o Hereditary Motor and Sensory Neuropathy (HMSN), nota anche come Neuropatia sensitivo-motoria ereditaria, è una sindrome neurologica ereditaria a carico del sistema nervoso periferico (neuropatia periferica). Deve il suo nome ai tre medici che per primi la descrissero: Jean-Martin Charcot, Pierre Marie, e Howard Henry Tooth.
| Malattia di Charcot-Marie-Tooth | |
|---|---|
 | |
| Malattia rara | |
| Cod. esenz. SSN | RFG060 |
| Specialità | neurologia |
| Eziologia | mutazione |
| Classificazione e risorse esterne (EN) | |
| OMIM | 311860 |
| MeSH | D002607 |
| MedlinePlus | 000727 |
| eMedicine | 1232386 e 315260 |
| Sinonimi | |
| Hereditary Motor and Sensory Neuropathy Neuropatia sensitivo-motoria ereditaria | |
| Eponimi | |
| Jean-Martin Charcot Pierre Marie Howard Henry Tooth | |
Con il nome CMT sono indicate molte malattie, i cui sintomi sono estremamente diversi: la forma di gran lunga più diffusa è la 1A, che si caratterizza per perdita di tono muscolare e della sensibilità al tatto, in particolare agli arti inferiori al di sotto del ginocchio; meno frequentemente, e in genere negli stadi più avanzati della malattia, gli effetti si notano anche negli arti superiori al di sotto del gomito. Allo stato attuale non esistono cure, sebbene la CMT sia la malattia più diffusa tra le sindromi neurologiche ereditarie, con 36 casi di insorgenza ogni 100.000 nascite[1]. A causa dei geni difettosi, la crescita della mielina dei nervi periferici risulta imperfetta e danneggiata causando danno all'assone.
In Italia è classificata dal Ministero della Sanità come malattia rara, sebbene sia probabilmente sottostimata, secondo alcuni studi. Prima di identificare i geni responsabili, era spesso considerata a metà tra le neuropatie e le miopatie primitive, come una variante della distrofia muscolare.
Decorso
modificaÈ una malattia progressiva cronica, curabile ma non guaribile, che può portare ad esiti completamente differenti: da insignificanti variazioni nelle capacità motorie all'atrofizzazione degli arti (che arrivano ad assumere una caratteristica forma assottigliata) con una serie di effetti correlati, da difficoltà di deambulazione e dolori muscolari fino (in rari casi) alla necessità permanente di sedia a rotelle. Non è una malattia letale e solo in alcuni casi rari e specifici la muscolatura respiratoria viene danneggiata. La neuropatia può rivelarsi anche in età adulta ma solitamente compare tra il primo e il secondo decennio di vita.
Diagnosi
modificaPer la diagnosi della sindrome esiste una linea guida approvata dalla SIN, la Società Italiana di Neurologia[2]. A grandi linee si può affermare che esistono moltissime varianti, che comportano diversi quadri clinici; la forma più diffusa è la "1A". Persone con la stessa variante possono presentare sintomi completamente diversi. Esistono molte forme di CMT e neuropatie ereditarie, molte con geni ancora sconosciuti e che spesso si presentano sotto diverse forme anche nella stessa famiglia, talvolta difficili da diagnosticare o non diagnosticate; a causa di ciò, la mancanza del gene specifico ricercato nel test del DNA può condurre a diagnosticare sia una neuropatia idiopatica o di altro tipo, sia di diagnosticare lo stesso la CMT o neuropatia genetica di altro tipo, in quanto l'assenza del gene determinante può non essere probante (vengono scoperti ogni anno nuovi geni e varianti di Charcot-Marie-Tooth).
Cura
modificaNonostante i progressi fatti dalla ricerca nello studio delle cause e del decorso della malattia, a oggi non esiste una cura specifica. Si ricorda che sotto il nome CMT vengono raggruppate molte malattie con decorso molto diverso. La riabilitazione ha dato ottimi risultati. Una combinazione di accorgimenti nello stile di vita e/o l'assunzione attenta di farmaci possono contribuire a rallentare e ridurre gli effetti della sindrome. È stato sperimentato sull'uomo il trattamento della forma 1A con acido ascorbico, con risultati non significativi. Attualmente è in fase di sperimentazione lo studio clinico PREMIER su un farmaco chiamato PXT3003. Lo studio è in fase III e i risultati sono attesi per la fine del 2023.
Trattamento delle deformità
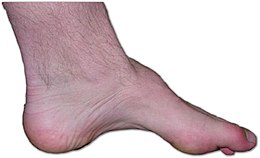
modificaPossono manifestarsi deformità progressive, in particolar modo a carico dei piedi, che risultano cavi, ma possono essere coinvolte anche le mani, la colonna vertebrale e le anche. Il trattamento in questi casi si avvale di riabilitazione, ortesi e chirurgia.
Tipi di CMT
modificaSulla base di differenze genetiche e sintomatiche si distinguono diversi tipi di patologia.
- CMT di tipo 1 (CMT1): demielinizzante con varianti; tale tipo si manifesta nell'80% dei casi di CMT ed è la più frequente. I sottotipi sono caratterizzati da sintomi comuni, come demielinizzazione, rilevabile attraverso la misurazione della velocità di conduzione nervosa. Si tratta di una patologia autosomica dominante.
- CMT di tipo 2 (CMT2): assonale; questa variante si manifesta circa nel 20% dei pazienti affetti da CMT. Anche la CMT di tipo 2 è una neuropatia autosomica dominante, che colpisce in modo preponderante l'assone. La velocità di conduzione nervosa (NCV) risulta lievemente ridotta, a volte invece nei limiti del normale.
- CMT di tipo 3 (CMT2) o sindrome di Dejerine-Sottas. NCV molto ridotta.
- CMT di tipo 4 (CMT4): molto rara, di tipo spinale o con sordità
- CMT di tipo 5: di tipo piramidale
- CMT di tipo 6: atrofia ottica, raro
- CMTDI: tipo autosomico intermedio dominante, raro
- CMTRI: tipo autosomico intermedio recessivo, raro
- CMT legata al cromosoma X (X-linked) (CMTX): la CMTX colpisce circa il 10-20% dei pazienti con CMT ed è di tipo dominante. Circa il 10% dei pazienti con CMTX presenta anche un'altra forma di CMT concomitante.
- CMT con blefaroptosi e parkinsonismo[3]
Il gene KIAA1840, conosciuto anche come ALS5 o SPG11, coinvolto con la CMT, in alternativa è altresì legato alla sclerosi laterale amiotrofica giovanile (malattia completamente diversa e più grave).[4]
Tutti e cinque i tipi sono caratterizzati da ulteriori sottotipi, discussi brevemente nella tabella.
| tipo | OMIM | gene | locus | descrizione |
| CMT1A | OMIM 118220 | PMP22 | 17p11.2 | La più comune forma di CMT (colpisce circa il 70-80% di pazienti con CMT di tipo 1). La NCV è media (15–20 m/s) e si presentano tremori ed atassia. |
| CMT1B | OMIM 118200 | MPZ | 1q22 | CMT causata da mutazioni sul gene che produce la proteina zero (P0), che colpisce circa il 5-10% dei pazienti con CMT di tipo 1. La NCV è media (<20 m/s) |
| CMT1C | LITAF | 16p13.1-p12.3 | CMT autosomica dominante che causa una grave demielinizzazione, evidente alla misurazione della NCV. Si manifesta solitamente a partire dall'infanzia, con sintomi identici alla CMT-1A. | |
| CMT1D | EGR2 | 10q21.1-q22.1 | La NCV è media (15–20 m/s) | |
| CMT2A | OMIM 118210 | MFN2 o KIF1B | 1p36 | Questa CMT è dovuta probabilmente ad una mutazione sulla proteina 2 della mitofusione. Alcune ricerche hanno invece correlato tale patologia a mutazioni sulla proteina kinesina 1B. I pazienti CMT2A non mostrano differenze di NCV, dal momento che la patologia è tipicamente assonale. |
| CMT2B | OMIM 600882 | RAB7 (RAB7A, RAB7B) | 3q21. | |
| CMT2B1 | LMNA | 1q22 | CMT assonale autosomica recessiva (laminopatia) | |
| CMT2C | OMIM 606071 | 12q23-q24 | Tale CMT può provocare debolezza a carico delle corde vocali e del diaframma. | |
| CMT2D | OMIM 601472 | GARS | 7p15 | I pazienti CMT2D, con mutazione a carico di GARS, tendono ad avere sintomi più gravi a carico delle estremità superiori (le mani), evento atipico per i pazienti CMT in genere. |
| CMT2E | NEFL | 8p21 | ||
| CMT2F | OMIM 606595 | HSPB1 | 7q11-q21 | |
| CMT2G | OMIM 608591 | 12q12-13 | ||
| CMT2H | OMIM 607731 | GDAP1 | 8q13-q21.1 | |
| CMT2J | OMIM 607736 | 1q22 | ||
| CMT2K | OMIM 607831 | 8q13-q21.1 | ||
| CMT2L | OMIM 608673 | 12q24 | ||
| CMT4A | OMIM 214400 | GDAP1 | 8q13-q21.1 | CMT autosomica recessiva |
| CMT4B1 | OMIM 601382 | MTMR2 | 11q22 | CMT autosomica recessiva |
| CMT4B2 | CMT4B2 (SBF2) | 11p15 | CMT autosomica recessiva. Il gene può anche essere chiamato "SBF2/MTMR13". | |
| CMT4C | KIAA1985 (SH3TC2) | 5q32 | CMT che può condurre a compromissione respiratoria. | |
| CMT4D | OMIM 601455 | NDRG1 | 8q24.3 | CMT autosomica recessiva, demielinizzante, caratterizzata da sordità |
| CMT1E | OMIM 118300 | PMP22 | 17p11.2 | CMT autosomica dominante, demielinizzante, caratterizzata da sordità[5] |
| CMT4E | EGR2 | 10q21.1-10q22.1 | "CMT4E" è un nome provvisorio | |
| CMT4F | PRX | 19q13.1-19q13.2 | "CMT4F" è un nome provvisorio, demielinizzante, assonale o spinale, a volte associata a PNH[6][7][8][9] | |
| CMT4J | OMIM 611228 | KIAA0274 (FIG4) | 6q21 | CMT autosomica recessiva |
| CMTX1 | OMIM 302800 | GJB1 | Xq13.1 | CMT caratterizzata da una NCV nella media. |
| CMTX2 | OMIM 302801 | Xq22.2 | ||
| CMT | OMIM 118301 | CMT con blefaroptosi e parkinsonismo | ||
| CMT | OMIM 302803 | CMT con aplasia cutis congenita di tipo 1 |
Neuropatia ereditaria con predisposizione alle paralisi da pressione
modificaLa neuropatia ereditaria con predisposizione alle paralisi da pressione (HNPP) è una neuropatia periferica genetica ereditaria, talvolta considerata una variante della malattia di Charcot-Marie-Tooth, con mononeuropatia ricorrente, scatenata da alcune attività fisiche solitamente innocue, come quelle che prevedono leggeri stress meccanici sul nervo (compressione, movimenti ripetuti o allungamento degli arti: es. accavallare le gambe, tenere le mani in posizioni innaturali a lungo, ecc.).[10]
Detta anche neuropatia tomaculare, è causata dal gene PMP22 del cromosoma 17p11.2 (lo stesso cromosoma dove presente il gene che causa il sottotipo CMT1E, caratterizzata da compromissione del nervo uditivo) ed è caratterizzata, anziché da classica demielinizzazione permanente, dalla membrana mielinica più spessa del normale in alcuni punti (tomacule). Nella HNPP si verificano paralisi temporanee in seguito a compressione del nervo, in quanto facilitate da tale malformazione della guaina che preme sull'assone.[5] La HNPP è generalmente causata dal gene PMP22 che codifica la proteina 22 della mielina periferica[11] del cromosoma 17p12[12] e secondariamente dalla mutazione della proteina Gly94fsX222 (c.281_282insG), causata dal gene PMP 22 del cromosoma 17p11.2 coinvolto nella CMT di tipo 1E. Nuove varianti genetiche diverse a livello di cromosoma vengono spesso scoperte come nel caso di molte neuropatie congenite.[13] Essa è chiamata anche coi nomi di paralisi da raccolta delle patate o da impianto dei bulbi di tulipano, poiché venne identificata la prima volta da Charcot, Marie e Tooth nel 1886 in una famiglia olandese dedita alla coltivazione dei tulipani.[10][13][14]
La diagnosi si basa essenzialmente sui sintomi manifesti, la diagnosi differenziale e l'anamnesi famigliare, poi il test genetico (positivo nell'80 % dei casi) ed eventualmente la biopsia al nervo. La HNPP insorge di solito nella seconda decade.[5] La velocità di conduzione nervosa, tranne nel sito interessato dalla compressione temporanea e lungo il nervo situato dopo di esso, risulta solitamente normale, per cui è difficile individuare la patologia con l'elettromiografia ed elettroneurografia, se la paralisi non è in corso o non ha causato atrofia da denervazione permanente o danni residui.[5]
Tra i segni, sintomi e condizioni associate: paralisi da pressione temporanee alle mani e braccia (sindrome del tunnel carpale, del tunnel cubitale (compressione del nervo ulnare) e radiale, con dolore, debolezza muscolare, parestesia, disestesia e perdita di sensibilità) che durano da alcuni minuti fino a giorni o mesi nei casi gravi, piede cadente temporaneo causato da paralisi da pressione del nervo peroneo comune[5], altre sindromi da compressione, crampi, tremore, astenia generale (leggera o media), alle braccia, alle gambe e alle dita delle mani, iporeflessia ai ginocchi, ipotonia muscolare con possibili deformità scheletriche (cifosi, piede cavo), radicolopatia, pseudo-sciatica, dolore neuropatico[15]
Una piccola percentuali di pazienti può sviluppare una polineuropatia con sintomi simili a quelli della CIDP o a tipologie di CMT.[5] Nell'80 % dei casi (forma benigna) vi è una delezione nel gene, mentre nel restante 20 % si verificano mutazioni puntiformi e una forma lentamente progressiva. Esistono diversi fenotipi di HNPP: mononeuropatia focale o multipla ricorrente, polineuropatia sensoriale cronica, polineuropatia sensorimotoria cronica tipo Charcot-Marie-Tooth-like/polineuropatia infiammatoria demielinizzante cronica-like, plessopatia brachiale monolaterale e deficit scapoloperoneale, più le forme insolite con coinvolgimento dei nervi cranici.[16]
Il paziente deve evitare alcune posizioni e può essere supportato con tutori ortopedici. Solitamente non dà mai grave disabilità.[5]
Neuropatia motoria ereditaria distale
modificaLa neuropatia motoria ereditaria distale presenta sintomatologia e coinvolgimento in comune con la SMA, e delle particolarità genetiche che le differenziano sia dalle SMA che dalle CMT.[17]
Note
modifica- ^ (EN) AA.VV. «Neurological dysfunction and axonal degeneration in Charcot-Marie-Tooth disease type 1A» (2000)
- ^ Linee guida per la diagnosi della Malattia di Charcot-Marie-Tooth e delle neuropatie correlate Archiviato il 1º gennaio 2008 in Internet Archive., dal sito neuro.it
- ^ OMIM 118301
- ^ Identificato il gene responsabile della malattia Charcot-Marie-Tooth
- ^ a b c d e f g Thomas D. Bird, Hereditary Neuropathy with Liability to Pressure Palsies, in GeneReviews(®), University of Washington, Seattle, 1º gennaio 1993. URL consultato il 6 agosto 2016.update 2014
- ^ Contactin-Associated Protein-Like 2-Related Peripheral Nerve Hyperexcitability Associated With Charcot-Marie-Tooth Type 4F
- ^ Pseudomyotonia and tetany in a familial neuropathy resembling Charcot-Marie-Tooth disease
- ^ Neuronal type of Charcot-Marie-Tooth Disease with a syndrome of contrinuous motor unit activity
- ^ Neuromyotonia in the spinal form of Charcot-Marie-Tooth disease
- ^ a b Neuropatia ereditaria con predisposizione alle paralisi da pressione, Orphanet
- ^ OMIM Entry - * 601097 - PERIPHERAL MYELIN PROTEIN 22; PMP22, su omim.org. URL consultato il 18 agosto 2016.
- ^ mapview, Map Viewer, su ncbi.nlm.nih.gov. URL consultato il 18 agosto 2016.
- ^ a b van Paassen, Barbara W; Kooi, Anneke J van der; Spaendonck-Zwarts, Karin Y van; Verhamme, Camiel; Baas, Frank; Visser, Marianne de (19 March 2014). "PMP22 related neuropathies: Charcot-Marie-Tooth disease type 1A and Hereditary Neuropathy with liability to Pressure Palsies". Orphanet Journal of Rare Diseases. 9 (1). ISSN 1750-1172. doi:10.1186/1750-1172-9-38. Retrieved 18 August 2016.
- ^ (EN) Kazunori Sango e Junji Yamauchi, Schwann Cell Development and Pathology, Springer Science & Business Media, p. 83, ISBN 978-4-431-54764-8. URL consultato il 18 agosto 2016.
- ^ Sintomi affini alla fibromialgia (dolori diffusi migranti, tensione muscolare, eccessiva reattività soggettiva a stimoli, calo di serotonina, discinesie muscolari leggere).
- ^ Neuropatie ereditarie da ipersensibilità alla pressione (neuropatia tomaculare o allantoidea)
- ^ Irobi, J; De Jonghe, P; Timmerman, V (2004). "Molecular genetics of distal hereditary motor neuropathies". Human Molecular Genetics. 13 (suppl 2): R195–R202. doi:10.1093/hmg/ddh226. PMID 15358725.
Bibliografia
modifica- (EN) Karen M. Krajewski, Richard A. Lewis, Darren R. Fuerst, Cheryl Turansky, Steven R. Hinderer, James Garbern, John Kamholz e Michael E. Shy. «Neurological dysfunction and axonal degeneration in Charcot-Marie-Tooth disease type 1A», da Brain. A Journal of Neurology, vol. 123, n° 7, 1516-1527, luglio 2000, Oxford University Press
- (EN) Paolo Vinci. Rehabilitation Management of Charcot-Marie-Tooth Disease, 2001. Testo allegato in italiano (Trattamento riabilitativo della malattia di Charcot-Marie-Tooth)
- (EN) P. Berger, P. Young e U. Suter. «Molecular Cell Biology of Charcot-Marie-Tooth Disease», in Neurogenetics 4:1-15. Berlin-Hannover, Springer 2002. ISSN 13646745 (stampa), ISSN 13646753 (rivista online).
- (EN) Fusco C, Frattini D, Pisani F, Spaggiari F, Ferlini A, Della Giustina E. "Coexistent Central and Peripheral Nervous System Involvement in a Charcot-Marie-Tooth Syndrome X-linked Patient" J Child Neurol. 2010 Apr 9. [Epub ahead of print]. [1]
- (EN) Fusco C, Frattini D, Scarano A, Della Giustina E. "Congenital pes cavus in a Charcot-Marie-Tooth disease type 1A newborn" Pediatr Neurol. 2009 Jun;40(6):461-4. [2]
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su malattia di Charcot-Marie-Tooth
Collegamenti esterni
modifica- (EN) Robert Joynt, Charcot-Marie-Tooth disease, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Sito dell'Associazione ACMT-Rete per la malattia di Charcot-Marie-Tooth, su acmt-rete.it.
- Sito dell'Associazione Italiana Charcot Marie Tooth, su aicmt.org.
- Sito della CMT di tipo 2A da Mitofusina 2, su progettomitofusina2.com.
- Sito della Federazione Europea di Associazioni CMT (in inglese), su ecmtf.org.
- Sito della Cmtaa Australia (in Inglese), su e-bility.com. URL consultato l'11 luglio 2006 (archiviato dall'url originale il 17 luglio 2006).
- Sito della Associazione CMT americana (in inglese), su charcot-marie-tooth.org. URL consultato il 10 febbraio 2007 (archiviato dall'url originale l'11 maggio 2008).
- Sito della Cmt France (in Francese), su cmt-france.net. URL consultato l'11 luglio 2006 (archiviato dall'url originale il 18 giugno 2006).
- Sito della Cmt Svizzera (in Tedesco), su cmt-schweiz.ch. URL consultato l'11 luglio 2006 (archiviato dall'url originale il 25 agosto 2006).
- Sito della Cmt United Kingdom (in Inglese), su cmt.org.uk.
- Sito dell'International CMT Organisations Usa/Canada (in Inglese), su hnf-cure.org.
- Sito dell Istituto Superiore di Sanità sulle malattie rare, su iss.it. URL consultato il 10 febbraio 2010 (archiviato dall'url originale il 27 febbraio 2011).
- CMT Central, su charcotmarietooth.org.
- Open Directory project, su dmoz.org.
- Trattamento chirurgico delle deformità nelle neuropatie periferiche, su ior.it. URL consultato il 10 settembre 2012 (archiviato dall'url originale il 28 marzo 2013).
- Modelli 3D dei muscoli della gamba:
- sketchfab.com, https://sketchfab.com/3d-models/leg-with-muscles-cc3585e0154a4060bebfb414dbcd7514.
- msdmanuals.com, https://www.msdmanuals.com/home/multimedia/3dmodel/muscular-system.
- innerbody.com, https://www.innerbody.com/anatomy/muscular/leg-foot.
- sketchfab.com, https://sketchfab.com/3d-models/anatomy-of-the-leg-da71907c71f64bfa86914744badda85f.
| Controllo di autorità | Thesaurus BNCF 52644 · LCCN (EN) sh85022641 · BNF (FR) cb122665167 (data) · J9U (EN, HE) 987007284792605171 |
|---|