「ヒドラジン」の版間の差分
編集の要約なし |
NipponDaemon (会話 | 投稿記録) |
||
| 128行目: | 128行目: | ||
{{Chem-stub}} |
{{Chem-stub}} |
||
{{DEFAULTSORT:ひとらしん}} |
{{DEFAULTSORT:ひとらしん}} |
||
[[Category:無機化合物]] |
[[Category:無機窒素化合物]] |
||
[[Category:窒素の化合物]] |
|||
[[Category:水素の化合物]] |
[[Category:水素の化合物]] |
||
[[Category:塩基]] |
[[Category:塩基]] |
||
2015年9月4日 (金) 20:03時点における版
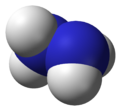
| ヒドラジン | |
|---|---|

|
|

| |
Hydrazine | |
別称 ヒドラジン ジアザン | |
| 識別情報 | |
| CAS登録番号 | 302-01-2 |
| PubChem | 9321 |
| ChemSpider | 8960 |
| UNII | 27RFH0GB4R |
| EC番号 | 206-114-9 |
| 国連/北米番号 | 2029 |
| KEGG | C05361 |
| MeSH | Hydrazine |
| ChEBI | |
| RTECS番号 | MU7175000 |
| バイルシュタイン | 878137 |
| Gmelin参照 | 190 |
| 3DMet | B00770 |
| |
| |
| 特性 | |
| 化学式 | H4N2 |
| モル質量 | 32.05 g mol−1 |
| 精密質量 | 32.037448138 g mol-2 |
| 外観 | 無色の液体 |
| 密度 | 1.013(8) g cm-3 |
| 融点 |
1 °C, 274 K, 34 °F |
| 沸点 |
114 °C, 387 K, 237 °F |
| 酸解離定数 pKa | 8.10[1] |
| 屈折率 (nD) | 1.46044 (at 22 °C) [2] |
| 粘度 | 0.876 cP |
| 構造 | |
| 双極子モーメント | 1.85 D[3] |
| 熱化学 | |
| 標準生成熱 ΔfH |
50.63 kJ mol-1(l)[4] |
| 標準モルエントロピー S |
121.21 J mol-1K-1 |
| 標準定圧モル比熱, Cp |
98.87 J mol-1K-1 |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 0281 |
| EU分類 | |
| EU Index | 007-008-00-3 |
| NFPA 704 | |
| Rフレーズ | R45, R10, R23/24/25, R34, R43, R50/53 |
| Sフレーズ | S53, S45, S60, S61 |
| 引火点 | 52 °C |
| 発火点 | 24–270 °C |
| 爆発限界 | 1.8–99.99 % |
| 半数致死量 LD50 | 59–60 mg/kg (経口:ラット、マウス)[5] |
| 関連する物質 | |
| 関連物質 | アンモニア |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ヒドラジン (hydrazine) は無機化合物の一種で、分子式 N2H4 と表される弱塩基。
アンモニアに似た刺激臭を持つ無色の液体で、空気に触れると白煙を生じる。水に易溶。強い還元性を持ち、分解しやすい。引火性があり、ロケットや航空機の燃料として用いられる。常温での保存が可能であるため、F-16戦闘機の非常用電源装置(EPU)やロシアなどのミサイルの燃料としても広く用いられており、また人工衛星や宇宙探査機の姿勢制御用の燃料としても使われている。プラスチック成形時の発泡剤、エアバッグ起爆剤、各種脱酸素剤として広く使用され、特に火力・原子力発電所用高圧ボイラーの防食剤として使用されている。 水加ヒドラジンは水素に代わる燃料電池の燃料としても模索されている。毒物。気化吸引、皮膚への接触ともに腐食をもたらす。また中毒症状をおこす。
水と共沸し、55 mol% のヒドラジンを含む混合物を与える。化学実験で用いる際は通常、抱水ヒドラジン (ヒドラジン一水和物、H2NNH2•H2O)が用いられる。
製法
アンモニアを次亜塩素酸塩で酸化するか、アンモニアを塩素で気相酸化して作る。
反応
ヒドラジンをカルボニル化合物と脱水縮合させると、ヒドラゾンが生じる。
- R-C(=O)-R' + H2NNH2 → R-C(=NNH2)-R' + H2O
ケトンを強アルカリ条件でヒドラジンとともに加熱すると、カルボニル基が還元を受けてメチレン基に変わる(ウォルフ・キッシュナー還元)。
- R-C(=O)-R' + H2NNH2 → R-CH2-R' + H2O + N2 (強アルカリ条件)
カルボン酸ハロゲン化物などのアシル化剤と反応し、ヒドラジドを与える。
- R-C(=O)-Cl + H2NNH2 → R-C(=O)-NHNH2
パラジウム触媒とともに用いると水素源となる。アルケンやニトロ基などを水素化してアルカンやアミノ基に変え、自身は窒素分子になる。このとき、中間体として生じるジアゼン (HN=NH) が高い還元力を持つ。
- Ar-NO2 + H2NNH2 → Ar-NH2 (パラジウム触媒下)
さまざまな酸とともに対応するヒドラゾニウム塩を生成する。2価の塩基として働き得るが、2段目のプロトン化は極めて弱い。
- N2H62+ N2H5+ + H+, pKa1 = -0.9
- N2H5+ N2H4 + H+, pKa2 = 8.10
関連項目
脚注
- ^ Hall, H.K., J. Am. Chem. Soc., 1957, 79, 5441.
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0070494398
- ^ グリーンウッド, ノーマン; アーンショウ, アラン (1997). Chemistry of the Elements (英語) (2nd ed.). バターワース=ハイネマン. ISBN 978-0-08-037941-8。
- ^ D.D. Wagman, W.H. Evans, V.B. Parker, R.H. Schumm, I. Halow, S.M. Bailey, K.L. Churney, R.I. Nuttal, K.L. Churney and R.I. Nuttal, The NBS tables of chemical thermodynamics properties, J. Phys. Chem. Ref. Data 11 Suppl. 2 (1982).
- ^ Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. Butterworth–Heinemann. pp. 361. ISBN 1903996651
- ^ ダイハツ 2007年9月14日ニュースリリース


