関節リウマチ
ウィキペディアは医学的助言を提供しません。免責事項もお読みください。 |
| 関節リウマチ | |
|---|---|
 | |
| 関節リウマチの影響を示した図 | |
| 概要 | |
| 診療科 | リウマチ学, 免疫学 |
| 分類および外部参照情報 | |
| ICD-10 | M05-M06 |
| ICD-9-CM | 714 |
| OMIM | 180300 |
| DiseasesDB | 11506 |
| MedlinePlus | 000431 |
| eMedicine | med/2024 emerg/48 pmr/124 |
| Patient UK | 関節リウマチ |
| MeSH | D001172 |
関節リウマチ(かんせつりうまち、Rheumatoid Arthritis:RA)は、自己の免疫が主に手足の関節を侵し、これにより関節痛、関節の変形が生じる代表的な膠原病の一つで、炎症性自己免疫疾患。
しばしば血管、心臓、肺、皮膚、筋肉といった全身臓器にも障害が及ぶ。
名称
以前は、「慢性関節リウマチ」と呼ばれ、第6回日本リウマチ学会総会(1962年)において「Rheumatoid Arthritis」の日本語訳が「慢性関節リウマチ」に決定されたが、「Rheumatoid Arthritis」という学名には「慢性」という語は一切含まれておらず、実際急性発症する例もあるため、これは完全な誤訳であるとする意見が多くあり、第46回日本リウマチ学会総会(2002年)において「関節リウマチ」を正式名称とする声明が発表された[1]。これに伴い、2006年、厚生労働省による特定疾患の名称も「関節リウマチ」に変更された[2]。
病因
- Mycoplasma fermentansは、GGPL-III抗原の研究から、RAの原因のひとつと推察されている[3]。
- ビオチン欠乏が一部の膠原病群の原因といわれている、ビオチン(「ビオチン欠乏により発症する病」の節)参照のこと
臨床像
関節炎
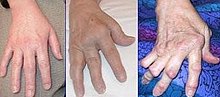
関節炎という言葉がわかりやすいので用いたが、実際に関節リウマチ患者におこるのは、関節の中でも特に滑膜がおかされ増殖する「滑膜炎」である。関節リウマチの患者は女性が多い。
初期には「朝のこわばり(morning stiffness)」と呼ばれる症状が出現する。朝起きてから、手をにぎることが困難であり、文字通りこわばっている。こわばりは、日によって違う場合がありひどい時で何も握れないなど症状はまばらである。5-10分程度のこわばりは他の疾患でも診られるが、1時間以上も続くこわばりであれば関節リウマチまたは他のリウマチ性疾患の可能性が高い。朝のこわばりのため、朝食の準備ができなくなる、シャツの釦を留められないなど生活に支障を来すことになる。昼頃にはたいてい改善している。また、症状の持続時間は関節リウマチそのものの活動性と関連している。すなわち1時間続く「朝のこわばり」より2時間続く「朝のこわばり」の患者の方が、関節リウマチが今まさに関節を破壊する強さが強い可能性がある。また、夜にもこわばりがあるというが関節リウマチとの因果関係は不明である。しかしながら万が一ということも考え医者の診察をしたほうが良いとされる。ただ夜のこわばりは、朝起床時と同様に体が休まっているなど条件が同じなためリウマチに大きく関係するとの論説もある。
そのうち、関節痛がおこるようになる。初期には手の指の関節(特に近位指節間関節)、また足の指の関節がおかされる。次第に手首、肘、膝など体の中心に近い大きな関節の痛みを感じるようになる。関節痛は、手を動かすなど活動すると増強する。そのため、強い関節炎があるとき、患者は自然とその関節を動かさないようにする傾向がある。
このような典型的な関節炎の症状のほか、関節リウマチは慢性に続く炎症であるため、全身倦怠感や易疲労感を持つ。
関節炎が進行すると、関節そのものが変性してゆく。関節にある滑膜細胞の増殖(パンヌス)、軟骨の破壊と骨にはびらんが生じる。最終的には関節という構造物が破壊し尽くされ、骨と骨が直接接した強直という状態になる。こうなるともはや関節を動かすことは出来ない。そのかわり、炎症も終息し痛みは感じない(炎症が起こる場であった滑膜が、完全に破壊され消失してしまったからである)。また、逆に関節が破壊された結果だらんだらんになることもあり、この場合ムチランス破壊と呼ばれる状態であるが強直よりもずっと頻度は低い。
指の骨が強直すると、最終的にスワンネック変形あるいはボタン穴変形といわれる典型的な関節リウマチ患者の手の形を呈する。尺側偏位もリウマチ患者によく見られる指が全て外側(尺骨側)を向く変形であるが、これは関節の脱臼が原因である。 指の変形において、DIPのみが変形を来たす場合は、ヘバーデン結節や乾癬性関節炎を念頭において、鑑別診断を下す。 また、筋肉と骨とをつなぐ腱の周囲に炎症がおよぶなどして腱断裂が生じることがある。これは突然発症し、無痛性である。腱が無くなれば、まさにそれに連続する筋肉を動かすことが出来なくなる。
手足の関節の他では、胸・腰の背骨はおかされないが首の背骨(頚椎)はおかされやすい。頚部痛を生じるか、または頚椎が亜脱臼し脊髄損傷を来す。 又、鎖骨には両端に関節がついており他の関節と同じように関節痛が起こる事もある。
血管
血管病変を合併する場合には、全身にくまなく留意しなければならない。レイノー現象は膠原病でよくみられる両側性の手指の虚血を示唆している。心臓では狭心症・心筋梗塞、肺では肺高血圧症、腎臓では糸球体硬化症、脳では脳梗塞が起こりうる。これらにより関節リウマチ患者の生命予後は、一般の日本人と比べて悪い。[4]
眼
関節リウマチ患者にはシェーグレン症候群が合併しやすく、乾燥性角結膜炎によるドライアイもよく見られる。目の内側にリウマトイド結節が生じることもある。(関節リウマチ患者の20%程度がシェーグレン症候群を合併するといわれている。)上強膜炎や強膜炎が見られることがあるが、強膜炎を発症している場合は通常その他の関節外症状も合併していることが多く、血管炎の一症状である可能性があり、悪性関節リウマチの診断を念頭におかねばならない。(悪性関節リウマチは公費負担対象の特定疾患である。)
呼吸器
間質性肺炎、気道病変、胸膜病変、リウマチ結節、血管病変、睡眠時無呼吸症候群(顎関節病変、輪状披裂関節病変)などを合併することがある。その病型は様々であるが、原因としては関節リウマチそのものによる合併症(リウマチ肺と呼ばれる)、感染症(特に肺結核・ニューモシスチス肺炎)、治療薬(特にメソトレキセート)による副作用など多岐にわたる。
心臓
心臓超音波検査を行うと心嚢液の貯留を認めるが、これは関節リウマチによる心膜炎の所見である。心臓にリウマトイド結節を生じることもある。
消化管
関節リウマチ自体は消化管をおかさないが、慢性の炎症によりAAアミロイドーシスが生じることがある。また、リウマトイド血管炎による虚血性腸炎はおこる可能性はある。いっぽう、非ステロイド系抗炎症鎮痛薬による胃潰瘍は比較的よく起こる。またメソトレキセートによる消化管の新陳代謝阻害により消化管出血を来すこともある。関節リウマチ患者は上部消化管内視鏡を定期的に受けた方が良い。
腎臓
関節リウマチ自体は腎臓をおかさないが、合併するシェーグレン症候群、ステロイドおよび非ステロイド系抗炎症鎮痛薬による間質性腎炎や金製剤・d-ペニシラミン、AAアミロイドーシスによる糸球体病変(膜性腎症が多い)がおこりうる。リマチル®はしばしば蛋白尿をおこすため検尿が行われる。
神経
関節リウマチに伴い血管炎が生ずれば、それに伴い多発単神経炎が起こる事がある。
皮膚
圧のかかる部位に、リウマチ結節と呼ばれる病変がみられることがある。皮下出血などもみられる。
血液
重症の関節リウマチ患者においては、脾腫、白血球(好中球のみ)減少をきたし、フェルティ症候群と呼ばれる病態を呈することがある。
検査
白血球増加、血小板増加、等の炎症所見が見られ、中でも特にC反応性蛋白(CRP)上昇、赤血球沈降速度亢進は活動性の指標となる。
リウマトイド因子(リウマチ因子、RF、RAテスト、RAHA、RAPA)は陽性であることがほとんどだが、関節リウマチがなくても陽性となるし、だれでも高齢となるにつれて陽性の頻度は高くなるからこれをもって診断を確定することは出来ない。また、活動性とは関連しないから経時的に測定することに意味はない。リウマトイド因子高値自体は重症の関節リウマチであることを示唆すると一般に言われているが、証明されたわけではない。より確実に診断につながる「抗CCP抗体」が、欧米では「リウマトイド因子」と組み合わせて用いられている。CA-RF(抗ガラクトース欠損IgG抗体)、IgG型リウマチ因子などもよく用いられてきている。関節破壊の指標としては「MMP-3」が用いられる。
リウマトイド血管炎を発症すれば補体が低下する。フェルティ症候群を発症すれば、白血球その他の血球が減少する。
画像診断
- 単純レントゲン写真…描出ではMRIに劣るが、簡便であり現在も用いられる。
- CT…滑膜、軟骨の描出でMRIに劣り、あまり用いられない。しかし最新の研究では、早期診断にて、CT法で足のX線所見と手関節または中手指節(MCP)関節の腫脹の所見を重視した上で、足の腫脹所見を加える手順に抗CCP抗体値の所見を組み込むことで陽性的中率は94.6%、陰性的中率は94.7%と高値を出せることがわかった。
- MRI…しばしば関節のびらん・破壊を評価するため用いられる。CTよりも軟骨病変・骨髄浮腫の評価に優れている。
- 超音波断層検査(エコー)…滑膜炎や骨髄浮腫像を検出出来ることが判明し、現在積極的に用いられることとなった。
診断
診断基準
旧来より、アメリカリウマチ学会(ARA、現在はACRと略す)の分類基準が、現在、関節リウマチの診断法として世界で一般的に使われている。
- ARAの分類基準(1987年)
- 朝のこわばり(一時間以上持続する)
- 多関節炎(少なくとも3領域以上の関節の腫れ)
- 手の関節の腫れ
- 対称性の関節の腫れ
- リウマチ結節
- リウマトイド因子(リウマチ因子)陽性
- レントゲン検査で典型的な関節所見
- 以上7項目のうち4項目以上を満たせば関節リウマチと診断される
しかし6週間未満でこれに基づく確定診断は不可能であるので、早期に診断するには、発症1年以内の早期関節リウマチの診断を目的に作成された、日本リウマチ学会の早期診断基準を使用する。この基準により、診断の感度は上がるが特異度は低下する。早期診断基準では、全身性エリテマトーデス・混合性結合組織病・ベーチェット病・乾癬性関節炎・強直性脊椎炎などの関節炎を起こす疾患を除外せねばならない。
近年、強力な抗リウマチ薬(特に抗サイトカイン療法)の登場によって、超早期の診断基準(関節のMRIや抗CCP抗体等)の確立が検討されている。
2009年、アメリカリウマチ学会年次学術集会で、上記に替わる新たな診断/分類基準として、アメリカとヨーロッパのリウマチ学会が共同で策定されが発表され、2010年8月、米国リウマチ学会(ACR)と欧州リウマチ学会(EULAR)の関節リウマチ新診断基準が23年ぶりの改定が発表された。[5]
- ACR/EULARの新診断基準(2010年)
- 関節浸潤 (0~5点)
- 抗体検査(RF または 抗CCP抗体) (0~3点)
- 炎症反応(CRP または ESR) (0~1点)
- 症状持続期間が6週間未満か (0~1点)
- 6点以上で関節リウマチと診断する。
活動性の評価
関節リウマチの病気を治癒させることはいまだできないものの、近年、その病気の勢いを抑え込んで、関節を破壊させないようにする治療法は既に現実のものとなっている。その場合、治療を進めていくにあたり活動性を評価する必要があり、ヨーロッパリウマチ連盟(EULAR)の提唱するDAS28や、アメリカリウマチ学会のACRコアセットを用いた評価基準(ACR20、ACR50、ACR70)が用いられる。ACRコアセットは臨床研究を主眼に置いたもので、その判定法はかなり煩雑である。また経時変化をみる相対的評価でもある。臨床の現場で用いるには、絶対評価であるDAS28のほうが現実的な評価法である。 血液検査では IgG-RFは活動性と相関するが、IgM-RFは相関しないといわれている。またCRP,MMP-3も活動性の指標となる。MMP-3>350では薬剤変更も視野におく。
病期分類
関節病期分類
「Steinbrocker Stage分類」により、最も進行した関節の単純X線画像・周囲組織所見からStage I~IVに分類される。「Larsen Grade分類」も用いられこちらは単純X線画像所見からGrade 0~Vに分類される。
ADL分類
「Steinbrocker Class分類」により、患者本人からの話・生活状況から判断しClass I~IVに分類される。近年ではHAQ(Health Assessment Quessionaire)が用いられることも多い。
治療
現在の治療指針では関節リウマチの診断がついたら、出来るだけ早期に抗リウマチ薬(DMARDs), 生物学的製剤を用いることが推奨されている。痛みに対する対症療法として非ステロイド系消炎鎮痛剤(NSAIDs)などを用いる。
DMARDs
関節リウマチの病気の勢いそのものを弱める薬として、メトトレキサート(リウマトレックス®)がはじめてEBMにのっとって効果がある薬と示された。さらにはスルファサラジン(アザルフィジン®)、ブシラミン(リマチル®)、レフルノミド(アラバ®)、ミゾリビン、タクロリムス(プログラフ®)が使用可能である。欧米では抗マラリア薬であるヒドロキシクロロキンもよく使用されるが、日本では適応がない。免疫抑制薬であるアザチオプリン(イムラン®)、シクロスポリン(ネオーラル®)も効果が示されているが、日本国内では適応はない。
DMARDsの特別な役割を理解するには、それまでのリウマチ治療の概念を理解しなければいけない。そもそも関節リウマチとは原因不明の疾患であって、関節が破壊されていくことを防ぐことはできず、ただただそのとき生じる痛みに対して対症療法を行うしかないと考えられていた。だから病歴が長く、体中の関節ががちがちに強直して寝たきりになった患者がいても、それは不十分な医療によるものではなく、むしろ医療の限界といえるものであった。それがDMARDsの出現によって、関節破壊の進行を遅らせることができるようになった。メトトレキサートの登場によって、関節リウマチの治療は180度の転向があったと言え、それはまさに抗TNF-α療法をも凌駕するほどのインパクトであった。
メトトレキセートには重篤な副作用がみられることがあり、慎重な対応が必要である。生命にかかわる副作用としては骨髄抑制と間質性肺炎がある。(ともに、まれであるが死亡例もある。)
- 骨髄抑制のチェックには血算・末梢白血球像を外来受診時に必ず行なうことが必要である。75歳以上では骨髄が破壊され、再生不能となることもある。高齢者へのメトトレキセートは推奨されない。プログラフ®を用いた方が良いとの意見もある。
- 間質性肺炎はメトトレキセートへのアレルギー反応と考えられており、処方開始後半年以内に発症例の85%が集中している。しかし4年経過した後に発症した例も報告されており、服用中は常に注意を要する。チェックには胸部レントゲン撮影・KL-6測定を用いる。
ステロイド
そもそもフィリップ・ショウォルター・ヘンチらが1950年代、世界ではじめてステロイド(糖質コルチコイド)の一種であるコルチゾンという物質を治療目的で関節リウマチ患者に投与したのである。これはまさに奇跡的な効果を発揮したと伝えられており、ステロイドの歴史は関節リウマチとともに始まったと言えるし、逆に関節リウマチの治療の歴史もステロイドとともに始まったのである。ヘンチはこのことでノーベル生理学・医学賞を受賞している。
ここしばらくのあいだ、DMARDsの疾患の進行を遅らせる効果が注目されていて、ステロイドにはそれはないとされた。ステロイドはしばらく、NSAIDsと同様の対症療法の薬として扱われていたのである。ステロイドの治療効果の発現は圧倒的に早いので、急性期に中等量用いられる程度のものであった。ステロイドは病気の進行を遅らせることはなく、副作用は強いので、維持的に投与すべきではないとされた。
今世紀に入って、これらの見方に転換が迫られている。臨床試験の結果、ステロイドもDMARDsと同様に、病気の進行を遅らせる効果を示すことがわかったからである。また、DMARDsのみよりもDMARDsにステロイドを加えたほうが病気の進行をさらに遅らせるという研究結果も報告され、懐疑的意見も強いものの、ステロイドは再び注目を集めている。
抗サイトカイン療法
インフリキシマブ(レミケード®)、アダリムマブ(ヒュミラ®)、トシリズマブ(アクテムラ®)、エタネルセプト(エンブレル®)、アバタセプト(オレンシア®)は新しく開発された薬で、これまでの製薬との違いとして、はじめからある機能を担うことを狙ってつくられた「分子標的薬」であることがあげられる。インフリキシマブとアダリムマブ、エタネルセプトについては抗サイトカイン療法でなく抗TNF-α療法と呼称されることもある。これらはリウマチに対してきわめて強力な治療効果を示し、リウマチの診療そのものの姿を変化させつつある。
一方欧米で承認されているアナキンラは日本では承認申請が行われていない。
我が国で認可された治療法は大阪大学免疫アレルギー内科のページに詳しい。
その他の研究段階の新しい治療法
そのほか、悪性リンパ腫に効果のあるリツキシマブ(リツキサン®)、抗生剤であるテトラサイクリン、高脂血症治療薬であるスタチン、多発性骨髄腫治療薬であるサリドマイドの効果や、造血幹細胞移植の効果も検討されている。 分子標的薬剤としてアバタセプトは米国では承認されている。
疾患そのものを治癒させることは可能か
他のリウマチ性疾患と同じく、原因そのものをなおす治療法は存在しない。しかし、最近の知見では発症早期(5年以内)からの抗サイトカイン療法によって、30~50%の症例で臨床的寛解(DAS28<2.6)が得られる事が分かってきており、なかでもインフリキシマブ(製品名: レミケード)においては、臨床的寛解に突入後、一定条件を満たす事ができれば投与を中止しても臨床的寛解がその後も持続する事が確認されている。この抗サイトカイン療法の中止に加えて、その他のDMARDs、ステロイド等を含む全ての治療薬を中止できた状態は「真の寛解」と呼ばれ、数年後の治療目標とされている。
