Khác biệt giữa bản sửa đổi của “Kali cyanide”
n Ccv2020 đã đổi Kali xyanua thành Kali cyanua: Tên bị Việt hóa quá mức. |
Sửa lỗi |
||
| Dòng 1: | Dòng 1: | ||
{{Thông tin hóa chất |
{{Thông tin hóa chất |
||
| |
| ImageFile = Kaliumcyanid.jpg |
||
| |
| ImageSize = 250px |
||
| ImageName = Mẫu kali cyanua |
|||
| ghi chú hình = |
|||
| |
| ImageFile1 = Potassium-cyanide-phase-I-unit-cell-3D-SF.png |
||
| ImageName1 = Cấu trúc của kali cyanua |
|||
| ghi chú hình 2 = Mô hình phân tử |
|||
| |
| Name = Kali cyanua |
||
| Section1 = {{Thông tin hóa chất/nhận dạng |
| Section1 = {{Thông tin hóa chất/nhận dạng |
||
| |
| CASNo = 151-50-8 |
||
| |
| EINECS = 205-792-3 |
||
| |
| RTECS = TS8750000}} |
||
}} |
|||
| Section2 = {{Thông tin hóa chất/thuộc tính |
| Section2 = {{Thông tin hóa chất/thuộc tính |
||
| Formula = KCN |
| Formula = KCN |
||
| |
| MolarMass = 65,1153 g/mol |
||
| Appearance = bột/tinh thể màu trắng |
|||
| ⚫ | |||
| |
| Density = 1,52 g/cm³ |
||
| ⚫ | |||
| MeltingPt = 634 °C |
|||
| Solubility = 71,6 g/100 ml (25 ℃) |
|||
}} |
|||
| MeltingPtC = 634}} |
|||
| Section4 = {{Thông tin hóa chất/nhiệt hóa học |
| Section4 = {{Thông tin hóa chất/nhiệt hóa học |
||
| |
| DeltaHf = -131,5 kJ/mol |
||
| |
| Entropy = 127,8 J·K<sup>-1</sup>·mol<sup>-1</sup>}} |
||
}} |
|||
| Section7 = {{Thông tin hóa chất/độc hại |
| Section7 = {{Thông tin hóa chất/độc hại |
||
| |
| ExternalMSDS = [http://www.inchem.org/documents/icsc/icsc/eics0671.htm ICSC 0671] |
||
| |
| EUIndex = 006-007-00-5 |
||
| |
| EUClass = Rất độc hại ('''T+''')<br>Nguy hiểm cho môi trường ('''N''') |
||
| |
| RPhrases = R26/27/28, R32<br>R50/53 |
||
| |
| SPhrases = S1/2, S7, S28, S29<br>S45, S60, S61 |
||
| |
| NFPA-H = 4 |
||
| |
| NFPA-F = 0 |
||
| |
| NFPA-R = 0 |
||
| |
| FlashPt = Không cháy |
||
| |
| LD50 = 5–10 mg/kg (miệng ở chuột, thỏ)<ref>Bernard Martel. ''Chemical Risk Analysis: A Practical Handbook''. Kogan, '''2004''', trang 361. ISBN 1-903996-65-1.</ref>}} |
||
}} |
|||
| Section8 = {{Thông tin hóa chất/liên quan |
| Section8 = {{Thông tin hóa chất/liên quan |
||
| |
| OtherCations = [[Natri cyanua]] |
||
| |
| OtherCpds = [[Hydro cyanua]]}}}} |
||
| ⚫ | '''Kali cyanua''' là tên gọi của một loại [[hợp chất|hợp chất hóa học]] không màu của [[kali]] có [[công thức hóa học]] '''KCN'''. Nó có mùi giống như mùi quả hạnh nhân, có hình thức bề ngoài giống như [[đường (hóa học)|đường]] và hòa tan nhiều trong nước. Là một trong số rất ít chất có khả năng tạo ra các phức chất của [[vàng]] (Au) hòa tan được trong nước, vì thế nó được sử dụng trong ngành [[kim hoàn]] để mạ hay đánh bóng bằng phương pháp hóa học. Đôi khi nó cũng được sử dụng trong ngành khai thác các mỏ vàng để tách vàng ra khỏi quặng vàng (mặc dù [[natri cyanua]] được sử dụng phổ biến hơn). Cho đến những năm thập niên 1970 nó còn được sử dụng trong thuốc diệt [[Bộ Gặm nhấm|chuột]]. |
||
}} |
|||
| ⚫ | '''Kali |
||
== |
==Tính chất hóa học== |
||
| ⚫ | |||
{{Wiki hóa}} |
|||
| ⚫ | |||
| ⚫ | |||
===Tính chất vật lý=== |
|||
[[Tinh thể]] màu trắng, thường ở dạng bột. |
|||
[[Nhiệt độ nóng chảy]]: 634 [[độ Celsius|°C]] |
|||
[[Khối lượng riêng]]: 1,52 g/cm<sup>3</sup> |
|||
[[Độ hòa tan]] (trong nước ở 25 °C): 71,6 g/100 g. |
|||
[[Phân tử khối]]: 65,12 đơn vị cacbon (đvC). |
|||
Không tan khi nhiệt độ môi trường dưới 0° |
|||
===Tính chất hóa học=== |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
==Các hiệu ứng sinh lý học và độc tính== |
==Các hiệu ứng sinh lý học và độc tính== |
||
===Độc tính=== |
===Độc tính=== |
||
Kali |
Kali cyanua là một chất cực độc, gây chết người với liều lượng thấp. Chỉ cần ăn nhầm từ 200–250 [[miligam|mg]] chất này thì một người khỏe mạnh có thể mất ý thức trong vòng 30 giây đến 2 phút. Sau khoảng 1 tiếng thì rơi vào trạng thái hôn mê và có thể tử vong sau khoảng 3 giờ nếu không có các biện pháp điều trị kịp thời. Theo phân loại trong hướng dẫn số 67/548/EEC của [[liên minh châu Âu]] thì nó là chất cực độc (T+). Giới hạn phơi nhiễm tối đa (PEL) của [[OSHA]] là 5 mg/m³. Còn theo quyết định số 3733/2002/QĐ-BYT ngày 10 tháng 10 năm 2002 của Bộ Y tế Việt Nam thì giới hạn này là 3 mg/m³ trong môi trường sản xuất. |
||
===Cơ chế ngộ độc=== |
===Cơ chế ngộ độc=== |
||
Giống như các hợp chất |
Giống như các hợp chất cyanua khác, kali cyanua gây độc bằng cách ngăn chặn sự trao đổi chất của tế bào. Kali cyanua có khả năng tạo liên kết hóa học với các [[heme]] trong máu (như [[hemoglobin]]), làm cho các tế bào không lấy được [[oxy]] và bị hủy hoại. Ngoài ra kali cyanua tác dụng với khí gas trong dạ dày tạo thành khí gas axit gây chết người khi hít phải. |
||
Các chất giải độc: |
Các chất giải độc: |
||
* Khi bị [[ngộ độc]] |
* Khi bị [[ngộ độc]] kali cyanua, cần sơ cứu nạn nhân bằng cách cho thở bằng khí oxy. Trong các phân xưởng có sử dụng cyanua kali, thường có sẵn bộ cấp cứu trong trường hợp nhiễm độc, bao gồm các chất [[amyl nitrit]], [[natri nitrit]], [[Xanh methylene|xanh metylen]] và [[natri thiosunfat]]. |
||
* Đường glucoza có khả năng làm chậm lại đáng kể quá trình gây độc của |
* Đường glucoza có khả năng làm chậm lại đáng kể quá trình gây độc của kali cyanua, đồng thời bảo vệ các tế bào bằng cách tạo liên kết hóa học với kali cyanua. |
||
===Các chỉ số an toàn=== |
===Các chỉ số an toàn=== |
||
Kali |
Kali cyanua không có các chỉ số an toàn rõ ràng. Tuy nhiên,nếu tiếp xúc với kali cyanua mà không có đồ bảo hộ (có thể thấm qua da) thì có thể gây ngộ độc và tỷ lệ cao là sẽ dẫn tới tử vong. |
||
==Chi tiết khác== |
==Chi tiết khác== |
||
Trong thực tế nhiều hợp chất |
Trong thực tế nhiều hợp chất kali được sử dụng trong các hóa chất tẩy rửa gia dụng. Tiêu chuẩn châu Âu thường kỹ càng hơn về các hợp chất kali so với các nước khác. Tuy nhiên ở Việt Nam loại độc chất này không phải ai cũng biết và thường được làm chất tẩy rửa chính trong các chất tẩy rửa đang lan tràn trên thị trường Việt Nam. Người Việt đang hít phải cả tấn thuốc độc. |
||
* Điều chế kali |
* Điều chế kali cyanua |
||
N<sub>2</sub> + CH<sub>4</sub> → HCN + NH<sub>3</sub> → NH<sub>4</sub>CN + KOH → KCN + NH<sub>3</sub> + H<sub>2</sub>O |
N<sub>2</sub> + CH<sub>4</sub> → HCN + NH<sub>3</sub> → NH<sub>4</sub>CN + KOH → KCN + NH<sub>3</sub> + H<sub>2</sub>O |
||
==Xem thêm== |
==Xem thêm== |
||
* [[ |
* [[Cyanua]] |
||
==Ghi chú== |
==Ghi chú== |
||
{{Tham khảo}} |
{{Tham khảo}} |
||
Phiên bản lúc 12:45, ngày 28 tháng 4 năm 2021
| Kali cyanua | |
|---|---|
 Mẫu kali cyanua | |
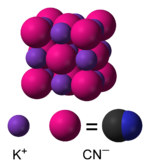 Cấu trúc của kali cyanua | |
| Nhận dạng | |
| Số CAS | |
| Số EINECS | |
| Số RTECS | TS8750000 |
| Thuộc tính | |
| Công thức phân tử | KCN |
| Khối lượng mol | 65,1153 g/mol |
| Bề ngoài | bột/tinh thể màu trắng |
| Khối lượng riêng | 1,52 g/cm³ |
| Điểm nóng chảy | 634 °C (907 K; 1.173 °F) |
| Điểm sôi | |
| Độ hòa tan trong nước | 71,6 g/100 ml (25 ℃) |
| Nhiệt hóa học | |
| Enthalpy hình thành ΔfH | -131,5 kJ/mol |
| Entropy mol tiêu chuẩn S | 127,8 J·K-1·mol-1 |
| Các nguy hiểm | |
| MSDS | ICSC 0671 |
| Phân loại của EU | Rất độc hại (T+) Nguy hiểm cho môi trường (N) |
| Chỉ mục EU | 006-007-00-5 |
| NFPA 704 |
|
| Chỉ dẫn R | R26/27/28, R32 R50/53 |
| Chỉ dẫn S | S1/2, S7, S28, S29 S45, S60, S61 |
| Điểm bắt lửa | Không cháy |
| LD50 | 5–10 mg/kg (miệng ở chuột, thỏ)[1] |
| Các hợp chất liên quan | |
| Cation khác | Natri cyanua |
| Hợp chất liên quan | Hydro cyanua |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Kali cyanua là tên gọi của một loại hợp chất hóa học không màu của kali có công thức hóa học KCN. Nó có mùi giống như mùi quả hạnh nhân, có hình thức bề ngoài giống như đường và hòa tan nhiều trong nước. Là một trong số rất ít chất có khả năng tạo ra các phức chất của vàng (Au) hòa tan được trong nước, vì thế nó được sử dụng trong ngành kim hoàn để mạ hay đánh bóng bằng phương pháp hóa học. Đôi khi nó cũng được sử dụng trong ngành khai thác các mỏ vàng để tách vàng ra khỏi quặng vàng (mặc dù natri cyanua được sử dụng phổ biến hơn). Cho đến những năm thập niên 1970 nó còn được sử dụng trong thuốc diệt chuột.
Tính chất hóa học
Nó có tính hoạt động hóa học cao:
- Dễ dàng phản ứng với các axit để tạo thành axit cyanic là chất độc dễ bay hơi.
- Từng được sử dụng trong công nghiệp tinh chế vàng.
Các hiệu ứng sinh lý học và độc tính
Độc tính
Kali cyanua là một chất cực độc, gây chết người với liều lượng thấp. Chỉ cần ăn nhầm từ 200–250 mg chất này thì một người khỏe mạnh có thể mất ý thức trong vòng 30 giây đến 2 phút. Sau khoảng 1 tiếng thì rơi vào trạng thái hôn mê và có thể tử vong sau khoảng 3 giờ nếu không có các biện pháp điều trị kịp thời. Theo phân loại trong hướng dẫn số 67/548/EEC của liên minh châu Âu thì nó là chất cực độc (T+). Giới hạn phơi nhiễm tối đa (PEL) của OSHA là 5 mg/m³. Còn theo quyết định số 3733/2002/QĐ-BYT ngày 10 tháng 10 năm 2002 của Bộ Y tế Việt Nam thì giới hạn này là 3 mg/m³ trong môi trường sản xuất.
Cơ chế ngộ độc
Giống như các hợp chất cyanua khác, kali cyanua gây độc bằng cách ngăn chặn sự trao đổi chất của tế bào. Kali cyanua có khả năng tạo liên kết hóa học với các heme trong máu (như hemoglobin), làm cho các tế bào không lấy được oxy và bị hủy hoại. Ngoài ra kali cyanua tác dụng với khí gas trong dạ dày tạo thành khí gas axit gây chết người khi hít phải.
Các chất giải độc:
- Khi bị ngộ độc kali cyanua, cần sơ cứu nạn nhân bằng cách cho thở bằng khí oxy. Trong các phân xưởng có sử dụng cyanua kali, thường có sẵn bộ cấp cứu trong trường hợp nhiễm độc, bao gồm các chất amyl nitrit, natri nitrit, xanh metylen và natri thiosunfat.
- Đường glucoza có khả năng làm chậm lại đáng kể quá trình gây độc của kali cyanua, đồng thời bảo vệ các tế bào bằng cách tạo liên kết hóa học với kali cyanua.
Các chỉ số an toàn
Kali cyanua không có các chỉ số an toàn rõ ràng. Tuy nhiên,nếu tiếp xúc với kali cyanua mà không có đồ bảo hộ (có thể thấm qua da) thì có thể gây ngộ độc và tỷ lệ cao là sẽ dẫn tới tử vong.
Chi tiết khác
Trong thực tế nhiều hợp chất kali được sử dụng trong các hóa chất tẩy rửa gia dụng. Tiêu chuẩn châu Âu thường kỹ càng hơn về các hợp chất kali so với các nước khác. Tuy nhiên ở Việt Nam loại độc chất này không phải ai cũng biết và thường được làm chất tẩy rửa chính trong các chất tẩy rửa đang lan tràn trên thị trường Việt Nam. Người Việt đang hít phải cả tấn thuốc độc.
- Điều chế kali cyanua
N2 + CH4 → HCN + NH3 → NH4CN + KOH → KCN + NH3 + H2O
Xem thêm
Ghi chú
- ^ Bernard Martel. Chemical Risk Analysis: A Practical Handbook. Kogan, 2004, trang 361. ISBN 1-903996-65-1.
Liên kết ngoài
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Kali cyanide. |
- International Chemical Safety Card 0671
- Hydrogen cyanide and cyanides (CICAD 61)
- National Pollutant Inventory - Cyanide compounds fact sheet
- NIOSH Pocket Guide to Chemical Hazards
- CSST (Canada) Lưu trữ 2013-11-02 tại Wayback Machine
- NIST Standard Reference Database
- Institut national de recherche et de sécurité (1997). "Cyanure de sodium. Cyanure de potassium Lưu trữ 2006-02-20 tại Wayback Machine". Fiche toxicologique n° 111, Paris:INRS, 6pp. (tiếng Pháp)

