سلسلة تنفس

سلسلة تنفس (الألمانية: Atmungskette وبالإنجليزية Breaching chain) هي جزء من الأيض وعلاقته بإنتاج الطاقة في جسم الإنسان وأغلب مملكة الحيوان. من ناحية، يصف تعبير «سلسلة تنفس» طريقا في عملية للتمثيل الغذائي، وهو تفاعلات كيميائية حيوانية من نوع تفاعلات أكسدة-اختزال (تبادل إلكترونات بين الجزيئات) تساعد الكائنات الحية على اكتساب الطاقة، ومن جهة أخرى تعني مجموع البروتينات التي تدخل في عملية الأيض. يتناول الإنسان الغذاء ويتنفس الأكسجين وعملية الأيض التي تتم عليهما تساعده على اكتساب الطاقة والنمو والقيام بوظائف الأعضاء. ولهذا فالتنفس مهم للحياة.
سلسلة التنفس الموصوفة هنا هي حالة خاصة تتم في متقدرات الخلايا وهي جزء من عملية الأيض ويشترك خلالها الأكسجين، تنتقل خلالها إلكترونات وتشكل من خلال تفاعلات كيميائية حيوية عملية أكسدة الفسفور في جزيئات ADP التي تحوي فوسفات يستخدمها الجسم لتخزين الطاقة مما يتناوله من غذاء. وعلى وجه التحديد يتحول أدينوسين ثنائي الفوسفات ADP بالأكسدة إلى أدينوسين ثلاثي الفوسفات ATP (إذ يكتسب ذرة فوسفور) ؛ يتم هذا التحول في متقدرات الخلايا لدى الإنسان وتمده بالطاقة. نفس الطريقة نجدها في مختلف الكائنات الحية.
عن طريق إلكترونات تقدمها مواد حيوية مثل NADH، و وFMNH2 وFADH2 تقوم عمليات أكسدة واختزال بالانتقال إلى مادة مؤكسدة. تلك المواد توجد في الغلاف الداخلي للمتقدرات. في كائنات حية مثل حقيقيات النوى تحدث روابط بين الهيدروجين (H2) والأكسجين (1/2 O2) ينتج منها ماء في الخلية على خطوات. فبدلا من أن ينشأ تفاعل شديد بينهما كما في حالة مخلوط انفجاري لإنتاج الحرارة تستغل الطاقة الناشئة من التفاعل بهدوء تكوين أدينوسين ثنائي الفوسفات ADP وفوسفات وهما اللذان يمدان الخلية الحية بالطاقة، ويتحولان إلى ثلاثي فوسفات الأدينوسين ATP ، وهي عملية تحدث فيها أكسدة الفوسفور.(جزيئات ATP تعطي الخلية العضلية طاقة لتتحرك وتؤدي وظيفتها.)
سلسلة التنفس هي حالة خاصة لسلسلة تنفس داخلية في المتقدرات، تنتقل خلالها إلكترونات، وهي تشكل عملية أكسدة الفوسفور من خلال عمليات كيميائية متتالية. الإلكترونات المرتبطة بالهيدروجين ومادتي NADH و FADH2 تعمل على أكسدة الأحماض الدهنية وتحلل السكر بواسطة دورة حمض الستريك.
سلسلة التنفس كسلسلة انتقال الإلكترونات
[عدل]تتكون سلسلة انتقال الإلكترونات من مجموعة جزيئات متتابعة لبعضها البعض، وهي تستطيع أخذ إلكترونات (تأكسد) أو إعطائها (عملية اختزال). تنتقل الإلكترونات عبر تلك السلسلة من مستويات طاقة عالية إلى مستويات طاقة منخفضة في الجزيئات، بحيث يصل الجزيء إلى محتوي منخفض للطاقة. في حقيقيات النوى توجد في سلسلة التفاعلات انزيمات المعقدات أربعة جزيئات I - IV ومواد تستطيع نقل الإلكترونات والهيدروجين و مرافق الإنزيم Q10 و Cytochrom c, وهي تكون موجودة في الغشاء الداخلي للمتقدرة وتشارك في عمليات انتقال الإلكترونات بهدف إنتاج ATP . البروتينات المشاركة في سلسلة انتقال الإلكترونات هي البروتينات المعقدة I–IV وبجانبها الجزيئات ناقلات الإلكترونات Ubichinon (أوبيكينون) وسيتوكروم سي وهي تشكل جميعا نظاما لتفاعلات أكسدة-اختزال (أكسدة جزيء يعني اكتساب جزيء لإلكترون، والاختزال - هو العملية العكسية - أن يفقد الجزيء إلكترونا). والهدف من تلك العمليات تكوين فرق للجهد الكهربائي حيث تتركز بروتونات فيما بين غشائي المتقدرة، مما يحفز أكسدة أدينوسين ثنائي الفوسفات ADP إلى أدينوسين ثلاثي الفوسفات ATP الذي يُختزن، ويمد الخلية بالطاقة عند احتياجها. فمثلا عندما يجري الإنسان تحتاج عضلاته إلى طاقة، تنتج تلك الطاقة من جزيئات الأدينوسين ثلاثي الفوسفات ATP - فهو حامل كثيف للطاقة، ويكون مخزونا في متقدرات الخلايا العضلية القائمة بالحركة. خلايا العضلات من الخلايا التي تحتوي على أعداد كبيرة من المتقدرات لتقوم بوظيفتها في التحريك، بالتالي تختزن الخلايا العضلية كثيرا من جزيئات ATP ، لاسغلالها وقت الحاجة، مثل الجري. هذا هو نظام توفير الطاقة في معظم الكائنات الحية.
خلال انتقال الإلكترونات من معقد (بروتين) لآخر تتغير تركيبة البروتينات وتتحرر بروتونات (هيدروجين ذو شحنة موجبة (H+)) وتخرج من متركس المتقدرة إلى المنطقة بين الغشائين الداخلي والخارجي للمتقدرة. فينشأ فرق جهد كهربائي (بسبب فرق تركيز البروتونات في خارج المتركس وداخله). الطاقة الناشئة من القوة الدافعة الكهربية الناشئة من الهيدروجين الموجب الشحنة يستغلها إنزيم ATP-Synthase لتكوين ادينوسين ثلاثي الفوسفات ATP من ادينوسين ثنائي الفوسفات ADP وفوسفور. لهذا تسمى سلسلة التنفس أيضا «فسفرة سلسلة التنفس».[1]
وظيفة المعقدات في سلسلة التنفس
[عدل]تحوي المتقدرة غشائين أحدهما خارجي والآخر داخلي، المنطقة المحصورة بينهما تلعب دورا هاما في سلسلة التنفس. من الأربعة معقدات IV - I تخترق ثلاثة منها الغشاء الداخلي، أما المعقد II يكون محصورا داخل الغشاء (أنظر الصورة 2). تنشأ تركيزات مختلفة للهيدروجين الموجب الشحنة بين داخل المتركس والمنطقة خارج الغشاء الداخلي، هذا الفرق في الجهد الكهربائي يستغله انزيم ATP-Synthase لتصنيع أدينوسين ثلاثي الفوسفات ATP .
المعقد I
[عدل]NADH: Ubiquinone- Oxidoreductase أو نازعة أن-أي-دي-إتش

الأوبيكينون هو (مرافق الإنزيم Q10)، وهو إنزيم معقد يتكون من 940 دالتون)، يُختزل بواسطة ثنائي نوكليوتيد الأدنين وأميد النيكوتين NAD+ خلال دورة حمض الستريك إلى Ubiquinol . ويتكون المعقد من جزئين يشكلان مع بعضهما البعض شكل حرف L . في أحد أجزائها نوكليوتيدات تحتوي على فلافين FMN ومراكز حديد وكبريت تحفز تفاعل أكسدة-أختزال. انتقال الإلكترونات الناشيء عن تفاعلات الأكسدة-اختزال تـُنتج من 3 إلى 4 بروتونات لكل جزيء NADH مؤكسد وتـُضخ هذه البروتونات إلى المنطقة بين الغشائين في المتقدرات.[2] فتتزايد الشحنات الموجبة فيما بين الغشائين، ويتكون مدرج جهد كهربائي بين خارج المتركس وداخله. الإلكترونات الناتجة من العملية تذهب إلى أوبيكينون في الغشاء الداخلي الذي يعطيها بدوره إلى المعقد III.
المعقد II
[عدل]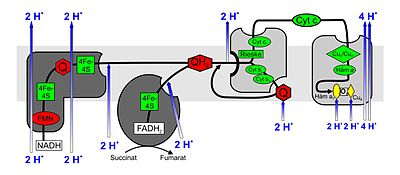
نازع هيدروجين السكسينات succinate dehydrogenase هو أنزيم يوجد في الخلية الحية ويساعد في سلسلة التنفس؛ يسمى أيضا «معقد II» في سلسلة التنفس، ويوجد في متقدرات الخلايا. زهو يوجد أيضا في خلايا الكثير من البكتيريا وحقيقيات النوى.
نازع هيدروجين السكسينات هو الإنزيم الوحيد الذي يشترك في العمليتين: دورة حمض الستريك وفي سلسلة نقل الإلكترونات في المتقدرات.[3] [4]
في الخطوة 6 في دورة حمض الستريك يقوم نازع هيدروجين السكسينات SQR بتخفيز أكسدة السكسينات إلى فومارات مع اختزال الأوبيكينون إلى أوبيكينول. وهذا يحدث في الغشاء الداخلي للمتقدرات عن طريق ترابط التفاعلين بعضهما البعض.
المعقد III
[عدل]انزيم سيتوكروم سي-ريدوكتاز (المعقد III) Cytochrom c–Oxidoreduktase): يقوم السيتوكروم سي بأكسدة جزيء الأوبكينون عبر دورة Q في داخل الغشاء الداخلي للمتقدرة باختزال جزيئين سيتوكروم سي موجودان في المنطقة المحصورة بين غشائي المتقدرة. والانزيم سيتوكروم سي-أوكسيداز (المعقد IV) يؤكسد 4 جزيئات «سيتوكروم سي» ويختزل في نفس الوقت جزيء أكسجين منتجا جزيئين من الماء.
المعقد IV
[عدل]
في المعقد IV يتأكسد سيتوكروم سي بمساعدة الإنزيم مؤكسد سيتوكروم سي، وفي نفس الوقت يُختزل الأكسجين إلى ماء. تستغل الطاقة الناتجة عن عملية أكسدة سيتوكروم سي في إنتاج بروتونات في متركس المتقدرة وتنتقل تلك البروتونات إلي المنطقة ما بين غشائي المتقدرة.
يعتبر إنزيم أيه تي بي سينثاز هو المعقد V (انظر الشكل 1). يبدأ تحفيز أكسدة ADP إلى ATP عند تواجد فرق الجهد الموجب في الوسط بين غشائي المتقدرة والمتركس. وتتم سلسلة التنفس بإنتاج أدينوسين ثلاثي الفوسفات ATP.
مثبطات سلسلة التنفس
[عدل]ما يميز المثبطات أنه لا ينتج عنها استهلاك للاكسجين حيث ان معدل الفوسفات إلى الاكسجين يضل ثابتا، وأنها ترتبط بالانزيمات أو مرافقات الانزيمات الخاضة بسلسلة التفس
يوجد العديد من ثبطات سلسلة التنفس:
- روتينون (Rotenone), والاموباربيتال (Amobarbital) التي تعيق عمل المعقد I، لكن لان نقل البروتونات ممكن ان يستمر عبر المعقد II، وبذلك تستمر سلسلة التنفس.
- المالونات تثبط المعقد II
- المضاد الحيوي انتي مايسين أ يثبط المعقد III ، حيث يعمل على منع انتقال الالكترونات من السيتوكروم بي إلى السيتوكروم سي 1 ، وبذلك تتأثر كل العوامل في المعقد III والمعقدات التي قبله، ممن ما يؤدي إلى تعطيل عمل المعقدات التي بعده كذلك.
- السيانيد والازيدات واول اكسيد الكربون تثبط المعقد IV حيث تعمل على حجز مكان ارتباط الاكسجين في المعقد. من ما يؤدي إلى تزاحم البروتونات، وفي الاخير إلى تعطيل سلسلة التنفس.
- المضاد الحيوي اولقو مايسين يثبط المعقد V حيث يرتبط بالجزء F0 مما يعيق انتقال البرتونات.
- ثنائيات الجوانيد مثل تلك التي تنتج عن الميتفورمين (دواء لمرض السكري) من المحتمل انها تثبط المعقد I.[5]
فاصلات سلسلة التنفس
[عدل]هي المركبات التي تعمل ازاحة الطاقة الغشائية لميتوكوندريوم (التدرج البروتيني). وبذلك يتم فصل الرابط ما بين تفاعل التأكسد وتفاعل الفسفرة. حيث لا يمكن إنتاج طاقة على هيئة ATP ثلاثي فوسفات الأدينوزين، ورغم ذلك فان استهلاك الاكسجين باقي والطاقة الناتجة تتحول إلى حرارة .الجدير بالذكر ان الجسم يقوم بصورة فيسلوجية (طبيعية) بفصل سلسلة التنفس للاستفادة من الحرارة الناتجة عن ذلك. ولهذا يمكن ان نقسم الفاصلات إلى نوعين:
- النوع الطبيعي (الفسليوجي): من الممكن للجسم ان ينتج بروتينات تعمل على بناء ثقب (Por) في الغشاء الخلوي الداخلي للميتوكوندريوم الذي يسمح للبروتونات ان تنتقل دون الاسفادة من ذلك في إنتاج ATP . وهناك سلسلة من البروتينات التي ينتجها الجسم لهذا الغرض تنطوي تحت مسمى البروتينات الفاصلة (uncoupling protein : UCP) منها الثرموقينين (Thermogenin: UCP1) الذي تنتجة الخلاياء الدهنية البنية، والبروتين الفاصل 3 (UCP3) الذي تنتجه العضلات.
- النوع المرضي (الباتلوجي)
- ثنائي نيترول الفينول من محبات الدهن التي يمكن ان تنبني في الغشاء الداخلي للميتوكوندريا،
- فالوموسين
اقرأ أيضا
[عدل]- تدرج بروتوني
- سرتوين
- أيض
- كيمياء حيوية
- دنا متقدرة
- ثلاثي فوسفات الأدينوسين
- فلافين مونو نوكليوتيد
- أيه تي بي سينثاز
- سيتوكروم سي
- نازع هيدروجين السكسينات
- هيم بيروكسيداز
مراجع
[عدل]- ^ Bruce Alberts u. a.: Molecular biology of the cell. 4. Auflage. New York 2002, S. 773–793
- ^ R. G. Efremov, R. Baradaran, L. A. Sazanov: The architecture of respiratory complex I. In: طبيعة. Band 465, Nummer 7297, Mai 2010, S. 441–445, doi:10.1038/nature09066. PMID 20505720.
- ^ Oyedotun KS، Lemire BD (مارس 2004). "The quaternary structure of the Saccharomyces cerevisiae succinate dehydrogenase. Homology modeling, cofactor docking, and molecular dynamics simulation studies". The Journal of Biological Chemistry. ج. 279 ع. 10: 9424–31. DOI:10.1074/jbc.M311876200. PMID:14672929.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - ^ webmaster (4 مارس 2009). "Using Histochemistry to Determine Muscle Properties". Succinate Dehydrogenase: Identifying Oxidative Potential. جامعة كاليفورنيا (سان دييغو). مؤرشف من الأصل في 2018-10-10. اطلع عليه بتاريخ 2017-12-27.
- ^ A.، Swanson, Todd (2010). Biochemistry, molecular biology, and genetics (ط. 5th ed). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. ISBN:9780781798754. OCLC:427608835. مؤرشف من الأصل في 2019-12-08.
{{استشهاد بكتاب}}:|طبعة=يحتوي على نص زائد (مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)
