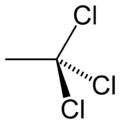
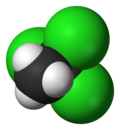
1,1,1-三氯乙烷
| 1,1,1-三氯乙烷 | |||
|---|---|---|---|
| |||
| IUPAC名 1,1,1-trichloroethane 1,1,1-三氯乙烷 | |||
| 系统名 1,1,1-三氯乙烷 | |||
| 别名 | 甲基氯仿 | ||
| 识别 | |||
| CAS号 | 71-55-6 | ||
| PubChem | 6278 | ||
| ChemSpider | 6042 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | UOCLXMDMGBRAIB-UHFFFAOYAP | ||
| ChEBI | 36015 | ||
| KEGG | C18246 | ||
| IUPHAR配体 | 5482 | ||
| 性质 | |||
| 化学式 | C2H3Cl3 或 CH3CCl3 | ||
| 摩尔质量 | 133.4 g·mol⁻¹ | ||
| 外观 | 無色液體 | ||
| 密度 | 1.32 g/cm³ (液體) | ||
| 熔点 | -33 °C (240 K) | ||
| 沸点 | 74 °C (347 K) | ||
| 溶解性(水) | 水溶性 | ||
| 危险性 | |||
| 警示术语 | R:R19, R20, R40, R59, R66 | ||
| 安全术语 | S:S9, S16, S24, S25, S46, S59, S61 | ||
| 主要危害 | 刺激上呼吸道,並可導致眼部出現嚴重的疼痛、發炎及腫塊。 | ||
| NFPA 704 | |||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
1,1,1-三氯乙烷是一種卤代烃(化學式:CH3CCl3或C2H3Cl3),是一种广泛应用的工業溶劑。其別名包括甲基氯仿及chlorothene,其商品名被称為溶劑 111及Genklene(帝國化學工業公司使用)。
歷史
[编辑]- 1840年:1,1,1-三氯乙烷由法國化學家亨利·维克托·勒尼奥 所發現。
- 1950年代至1995年:化學工業公司將其大量生產。時至今日,它已受蒙特利爾公約禁止及限制其應用。
生產
[编辑]在工業中,氯乙烯會用作生產1,1,1-三氯乙烷,一般需經兩個過程所生產。第一步驟,氯乙烯會於20 - 50°C跟鹽酸進行反應,生成1,1-二氯乙烷,催化劑有氯化鋁或氯化鋅。以下是該反應化學方程式:
- CH2=CHCl + HCl → CH3CHCl2
接著,1,1-二氯乙烷於紫外綫輻射下跟氯進行反應會轉化為1,1,1-三氯乙烷:
- CH3CHCl2 + Cl2 → CH3CCl3 + HCl
以上反應會生成約 80-90% 生成物及副生成物鹽酸可在第一個步驟重用。最多的副产物为1,1,2-三氯乙烷,1,1,1-三氯乙烷可透過蒸餾法分離。
1,1-二氯乙烯与氯化氫反應會生成少量1,1,1-三氯乙烷,最常見的催化劑是氯化鋁:
- CH2=CCl2 + HCl → CH3CCl3
用途
[编辑]1,1,1-三氯乙烷除了在眾多有機化合物中是屬於一種頗良好的溶劑,亦是一種含有最少毒素鹵素碳烴化合物。在《蒙特利爾公約》生效前,它可用作清潔金屬及印刷電路板,於電子業用作照片抗蝕溶劑,可作為氣霧劑推進器或切削液添加劑,也是一種除去墨水、印刷、膠黏劑及其他塗層的溶劑。它能安全有效地把在聚氯乙烯器皿中放置多年的銅及銀硬幣移除聚氯乙烯。
1,1,1-三氯乙烷擁有一種特性,它在清潔大部分攝影底片(電影/幻燈片等)時,不但沒有軟化其底片,還不會破壊清潔中的底片的感光乳劑。而其他一股的溶劑卻會破壞感光乳劑,因此,它們不能用來清潔底片。
Forane 141是一種可代替1,1,1-三氯乙烷的溶劑,可是其功效並不高,而且用後會留有殘餘物。
1,1,1-三氯乙烷很多的用途(包括清潔攝影底片等)在以前都採用四氯化碳,但亦已於1970年禁止使用。
蒙特利爾公約中提出1,1,1-三氯乙烷是其中一種負責消耗臭氧的化合物,以及於1996年起禁止、限制其用途。此後,它的使用以致生產都被全球各地逐步淘汰。[1]
1,1,1-三氯乙烷通常被視為非極性溶劑,但因為該三个電負性高的氯原子位於分子的同一邊,因而稍微帶有極性,使它能成為一優良溶劑相對於那些不能於完全非極性物質(例如:己烷)溶解的有機物質。1,1,1-三氯乙烷在實驗分析論中會由其它溶劑代替。
安全
[编辑]雖然1,1,1-三氯乙烷的毒性不及大部分相類似的化合物,但吸入或進食1,1,1-三氯乙烷對中樞神經系統會有鎮靜的作用及其所產生影響會跟中毒相似,包括頭昏眼花、混淆及在高濃度下會失去知覺,甚至死亡。
液態1,1,1-三氯乙烷與皮膚長時間接觸會除去皮膚上的脂肪,使皮膚受到慢性的刺激。
在研究實驗動物時,顯示1,1,1-三氯乙烷不會長時間殘留於體內。然而,長期接觸會導致肝臟、腎臟及心臟畸形。孕婦應避免接觸此等化合物,因為這樣會導致嬰兒畸形。
1,1,1-三氯乙烷對於昆蟲是致命的。
參考資料及注釋
[编辑]- ^ 耗盡臭氧物質於實驗中的用途 (PDF). [2008-05-14]. (原始内容 (PDF)存档于2008-02-27).
外部連結
[编辑]- http://www.informaworld.com/smpp/content?content=10.1006/enfo.2000.0011(页面存档备份,存于互联网档案馆)
- https://web.archive.org/web/20080509103329/http://www.atsdr.cdc.gov/toxprofiles/tp70.html
|
| |||||||||||||||||||||||||||||||||||||